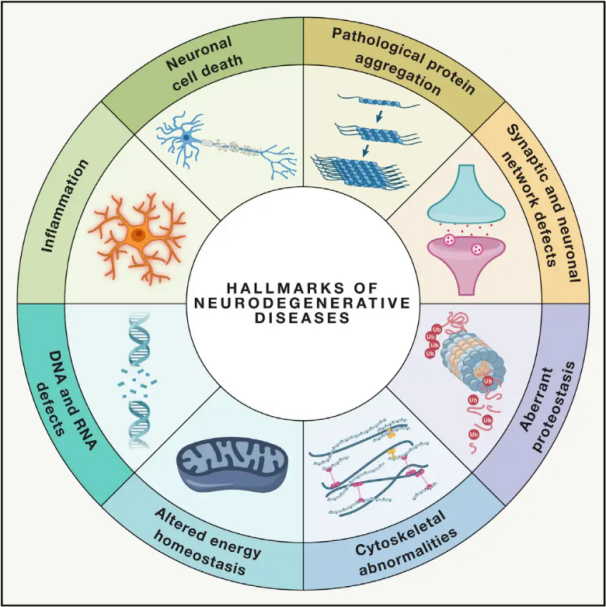
Enfermedades neurodegenerativasLas enfermedades neurodegenerativas (END) se caracterizan por la pérdida progresiva o persistente de poblaciones neuronales vulnerables específicas en el cerebro o la médula espinal. La clasificación de las END puede basarse en diversos criterios, como la distribución anatómica de la neurodegeneración (por ejemplo, trastornos extrapiramidales, degeneración frontotemporal o ataxias espinocerebelosas), anomalías moleculares primarias (como amiloide-β, priones, tau o α-sinucleína) o características clínicas principales (como la enfermedad de Parkinson, la esclerosis lateral amiotrófica y la demencia). A pesar de estas diferencias en la clasificación y la presentación de los síntomas, enfermedades como la enfermedad de Parkinson (EP), la esclerosis lateral amiotrófica (ELA) y la enfermedad de Alzheimer (EA) comparten procesos subyacentes comunes que conducen a la disfunción neuronal y, finalmente, a la muerte celular.
Con millones de personas afectadas en todo el mundo por enfermedades neurodegenerativas (END), la Organización Mundial de la Salud estima que para 2040, estas enfermedades se convertirán en la segunda causa principal de muerte en los países desarrollados. Si bien existen diversos tratamientos disponibles para aliviar y controlar los síntomas asociados con enfermedades específicas, aún no se han encontrado métodos eficaces para ralentizar o curar la progresión de estas afecciones. Estudios recientes indican un cambio en los paradigmas de tratamiento, pasando del mero manejo sintomático a la utilización de mecanismos de protección celular para prevenir un mayor deterioro. Numerosas evidencias sugieren que el estrés oxidativo y la inflamación desempeñan un papel fundamental en la neurodegeneración, lo que posiciona a estos mecanismos como objetivos críticos para la protección celular. En los últimos años, la investigación básica y clínica ha revelado el potencial de la terapia de oxígeno hiperbárico (TOHB) en el tratamiento de las enfermedades neurodegenerativas.
Comprensión de la terapia de oxígeno hiperbárico (TOHB)
La oxigenoterapia hiperbárica (OHB) generalmente implica aumentar la presión a más de 1 atmósfera absoluta (ATA) —la presión a nivel del mar— durante 90 a 120 minutos, requiriendo a menudo varias sesiones según la afección específica que se esté tratando. La mayor presión atmosférica mejora el suministro de oxígeno a las células, lo que a su vez estimula la proliferación de células madre y potencia los procesos de curación mediados por ciertos factores de crecimiento.
Originalmente, la aplicación de la oxigenoterapia hiperbárica (OHB) se basaba en la ley de Boyle-Marriott, que postula la reducción de burbujas de gas dependiente de la presión, junto con los beneficios de los altos niveles de oxígeno en los tejidos. Se sabe que diversas patologías se benefician del estado hiperóxico producido por la OHB, incluyendo tejidos necróticos, lesiones por radiación, traumatismos, quemaduras, síndrome compartimental y gangrena gaseosa, entre otras enumeradas por la Sociedad de Medicina Submarina e Hiperbárica. Cabe destacar que la OHB también ha demostrado eficacia como tratamiento coadyuvante en diversos modelos de enfermedades inflamatorias o infecciosas, como la colitis y la sepsis. Dados sus mecanismos antiinflamatorios y oxidativos, la OHB ofrece un potencial significativo como vía terapéutica para las enfermedades neurodegenerativas.
Estudios preclínicos de la terapia de oxígeno hiperbárico en enfermedades neurodegenerativas: Perspectivas del modelo de ratón 3×Tg
Uno de los estudios notablesEl estudio se centró en el modelo de ratón 3×Tg de la enfermedad de Alzheimer (EA), que demostró el potencial terapéutico de la oxigenoterapia hiperbárica (OHB) para mejorar los déficits cognitivos. La investigación incluyó ratones 3×Tg machos de 17 meses de edad, comparados con ratones C57BL/6 machos de 14 meses que sirvieron como grupo de control. El estudio demostró que la OHB no solo mejoró la función cognitiva, sino que también redujo significativamente la inflamación, la carga de placa y la fosforilación de Tau, un proceso crítico asociado con la patología de la EA.
Los efectos protectores de la oxigenoterapia hiperbárica (OHB) se atribuyeron a una disminución de la neuroinflamación. Esto se evidenció por la reducción de la proliferación microglial, la astrogliosis y la secreción de citocinas proinflamatorias. Estos hallazgos resaltan el doble papel de la OHB: mejorar el rendimiento cognitivo y, al mismo tiempo, mitigar los procesos neuroinflamatorios asociados con la enfermedad de Alzheimer.
Otro modelo preclínico utilizó ratones tratados con 1-metil-4-fenil-1,2,3,6-tetrahidropiridina (MPTP) para evaluar los mecanismos protectores de la oxigenoterapia hiperbárica (OHB) sobre la función neuronal y las capacidades motoras. Los resultados indicaron que la OHB contribuyó a mejorar la actividad motora y la fuerza de agarre en estos ratones, lo que se correlacionó con un aumento en la señalización de la biogénesis mitocondrial, específicamente a través de la activación de SIRT-1, PGC-1α y TFAM. Esto subraya el papel fundamental de la función mitocondrial en los efectos neuroprotectores de la OHB.
Mecanismos de la oxigenoterapia hiperbárica en enfermedades neurodegenerativas
El principio fundamental de la oxigenoterapia hiperbárica (OHB) para las enfermedades neurodegenerativas radica en la relación entre la reducción del suministro de oxígeno y la susceptibilidad a los cambios neurodegenerativos. El factor inducible por hipoxia-1 (HIF-1) desempeña un papel central como factor de transcripción que permite la adaptación celular a la baja tensión de oxígeno y se ha relacionado con diversas enfermedades neurodegenerativas, como la enfermedad de Alzheimer, la enfermedad de Parkinson, la enfermedad de Huntington y la esclerosis lateral amiotrófica, lo que lo convierte en una diana farmacológica crucial.
Dado que la edad es un factor de riesgo importante para múltiples trastornos neurodegenerativos, es vital investigar el impacto de la oxigenoterapia hiperbárica en la neurobiología del envejecimiento. Los estudios han indicado que la oxigenoterapia hiperbárica puede mejorar los déficits cognitivos relacionados con la edad en personas mayores sanas.Además, los pacientes ancianos con importantes problemas de memoria mostraron mejoras cognitivas y un aumento del flujo sanguíneo cerebral tras la exposición a la oxigenoterapia hiperbárica.
1. Impacto de la oxigenoterapia hiperbárica en la inflamación y el estrés oxidativo.
La oxigenoterapia hiperbárica (OHB) ha demostrado su capacidad para aliviar la neuroinflamación en pacientes con disfunción cerebral grave. Posee la capacidad de reducir las citocinas proinflamatorias (como IL-1β, IL-12, TNFα e IFNγ) y aumentar las citocinas antiinflamatorias (como IL-10). Algunos investigadores proponen que las especies reactivas de oxígeno (ERO) generadas por la OHB median varios efectos beneficiosos de la terapia. En consecuencia, además de su acción reductora de burbujas dependiente de la presión y el logro de una alta saturación de oxígeno tisular, los resultados positivos asociados a la OHB dependen en parte de las funciones fisiológicas de las ERO producidas.
2. Efectos de la oxigenoterapia hiperbárica sobre la apoptosis y la neuroprotección.
Las investigaciones han indicado que la oxigenoterapia hiperbárica (OHB) puede reducir la fosforilación de la proteína quinasa activada por mitógeno p38 (MAPK) en el hipocampo, mejorando así la cognición y disminuyendo el daño hipocampal. Se ha observado que tanto la OHB sola como en combinación con extracto de Ginkgo biloba reducen la expresión de Bax y la actividad de la caspasa-9/3, lo que resulta en una disminución de las tasas de apoptosis en modelos de roedores inducidos por aβ25-35. Además, otro estudio demostró que el preacondicionamiento con OHB induce tolerancia a la isquemia cerebral, mediante mecanismos que implican un aumento de la expresión de SIRT1, junto con un aumento de los niveles de la proteína Bcl-2 y una reducción de la caspasa-3 activa, lo que subraya las propiedades neuroprotectoras y antiapoptóticas de la OHB.
3. Influencia de la HBOT en la circulación yNeurogénesis
La exposición de los sujetos a la oxigenoterapia hiperbárica (OHB) se ha asociado con múltiples efectos en el sistema vascular craneal, incluyendo el aumento de la permeabilidad de la barrera hematoencefálica, la promoción de la angiogénesis y la reducción del edema. Además de proporcionar un mayor suministro de oxígeno a los tejidos, la OHBfavorece la formación vascularmediante la activación de factores de transcripción como el factor de crecimiento endotelial vascular y mediante la estimulación de la proliferación de células madre neurales.
4. Efectos epigenéticos de la oxigenoterapia hiperbárica
Los estudios han revelado que la exposición de células endoteliales microvasculares humanas (HMEC-1) al oxígeno hiperbárico regula significativamente 8.101 genes, incluyendo expresiones tanto aumentadas como disminuidas, lo que pone de manifiesto un aumento en la expresión génica asociada a las vías de respuesta antioxidante.
Conclusión
El uso de la oxigenoterapia hiperbárica (OHB) ha experimentado avances significativos con el tiempo, demostrando su disponibilidad, fiabilidad y seguridad en la práctica clínica. Si bien la OHB se ha explorado como tratamiento no autorizado para trastornos neurodegenerativos y se han realizado algunas investigaciones, sigue existiendo una necesidad imperiosa de estudios rigurosos para estandarizar las prácticas de OHB en el tratamiento de estas afecciones. Es fundamental realizar más investigaciones para determinar las frecuencias de tratamiento óptimas y evaluar el alcance de los efectos beneficiosos para los pacientes.
En resumen, la confluencia de la oxigenoterapia hiperbárica y las enfermedades neurodegenerativas demuestra una frontera prometedora en las posibilidades terapéuticas, lo que justifica su continua exploración y validación en entornos clínicos.
Fecha de publicación: 16 de mayo de 2025

